Le médicament, un secteur innovant
Chaque année, des avancées médicales redessinent les frontières de la médecine et marquent des tournants décisifs.
L’hépatite C, autrefois une maladie chronique difficilement guérissable, peut désormais être éliminée chez plus de 95 % des patients en seulement quelques semaines, grâce à des traitements révolutionnaires dont le premier a été disponible fin 2016.
Plus récemment, c’est la mucoviscidose qui a fait un saut de géant. Ce qui était autrefois une maladie mortelle devient, pour la majorité des malades, une pathologie chronique maîtrisée grâce à une nouvelle thérapie.
Et ces derniers mois, le traitement préventif contre la bronchiolite a considérablement réduit les hospitalisations des nourrissons, offrant un soulagement pour des milliers de familles. Les avancées dans les thérapies géniques permettent de traiter des maladies rares et génétiques, comme l’amyotrophie spinale, en ciblant directement les causes sous-jacentes au niveau moléculaire. Mais il ne faut jamais l’oublier : toutes ces innovations sont le fruit d’un travail colossal de recherche en amont.
Le parcours du médicament est long, risqué et coûteux et s’articule autour de trois grandes étapes :
➜ La recherche au cours de laquelle des milliers de molécules sont soumises à une batterie de tests afin d’étudier leurs propriétés chimiques et pharmacologiques et repérer celles qui pourraient avoir un intérêt thérapeutique. L’objectif est d’identifier des molécules qui, en fonction des découvertes de la recherche fondamentale, pourront répondre à un besoin médical, lutter contre une maladie, ou encore améliorer la qualité de vie des patients.
➜ Les essais pré-cliniques pour sélectionner une molécule ayant un intérêt thérapeutique potentiel et qui pourrait devenir un médicament. Ces tests sont réalisés sur des cellules (in vitro) et des animaux (in vivo). L’objectif est double : évaluer l’innocuité, la tolérance et l’efficacité du nouveau médicament sur plusieurs modèles, à ses différents stades de développement, et déterminer les doses à administrer à l’homme lors de la première phase d’essais cliniques.
➜ Le développement clinique et pharmaceutique pour tester le candidat médicament sur l’homme par la réalisation d’essais cliniques. La phase 1 teste la tolérance/ innocuité. La phase 2 permet d’évaluer l’efficacité du produit et de définir la dose optimale. Enfin, au cours de la phase 3 (études « pivots »), le médicament est administré à plusieurs centaines, voire milliers, de patients, afin d’apprécier son efficacité et sa bonne tolérance.
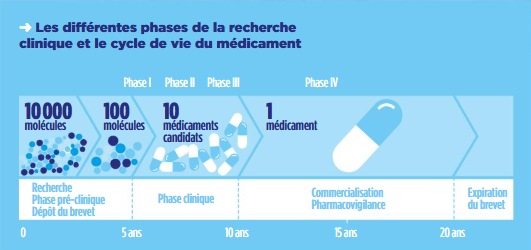
En moyenne, on estime qu’il faut tester entre 5 000 et 10 000 molécules pour qu’une seule atteigne finalement le marché en tant que médicament approuvé.
L’activité de recherche ne faiblit pas dans l’industrie pharmaceutique. Parmi les 271 AMM approuvées par l’Agence européenne du médicament entre 2021 et mi 2023, 45 % ont concerné des nouvelles substances actives.
Activité de recherche clinique et nouvelles molécules pour 2027
- 1 787 programmes de recherche clinique au 28/07/23
- 1 127 médicaments en développement (ciblant environ 600 mécanismes d’action différents)
- 660 nouvelles molécules potentielles d’ici 2027
Retrouvez notre Horizon Scanning 2024 « Avec quels médicaments serons-nous soignés demain ? » en intégralité : Horizon scanning 2024 - "Avec quels médicaments serons-nous soignés demain ?" | Leem

