La microfluidique
De quoi parle-t-on ?
Elle permet de fabriquer des laboratoires sur puces (lab on chip), qui sont de véritables laboratoires miniaturisés d'à peine 1 ou 2 centimètres, permettant de faire des analyses très rapides, avec un minimum de réactifs.
A titre d'exemple, on peut dire que la réalisation de séquenceurs d'ADN serait impossible sans la microfluidique.
Définition
Un fluide est un milieu matériel infiniment déformable. On regroupe sous cette appellation les liquides et les gaz, et par extension, dans le cadre de cette fiche, le sang, l'eau, l'huile, les suspensions cellulaires, les échantillons d'ADN...
Ce domaine de recherche en plein essor s'inspire souvent de l'observation de la nature, laquelle maîtrise parfaitement les écoulements de fluides dans des microcanaux.
L'arbre, un exemple de système microfluidique. Il draine la sève vers des milliers de feuilles, de manière homogène, en s'appuyant sur un réseau de millions de petits capillaires, dont les diamètres varient entre des centaines de microns et une trentaine de nanomètres. Il existe dans l'arbre des milliers de vannes intégrées qui préviennent la formation d'une embolie généralisée.
L'intérêt de la microfluidique
1. Elle permet d'accélérer les diagnostics et les analyses réalisées à partir de fluides. Dans une goutte de sang, par exemple, on peut obtenir en quelques minutes le TSH (thyréostimuline), différents taux d'hormone, identifier des pathogènes et réaliser en quelques heures un séquençage d'ADN et d'ARN.
2. Elle permet de mener massivement en parallèle plusieurs analyses.
3. Elle effectue des analyses à partir de très petites quantités d'échantillon, une cellule unique "single cell" par exemple.
4. Elle fait baisser les coûts d'analyse.
Ce qui se profile d'ici 2030
Une médecine personnalisée : la microfluidique permettra d'identifier, au sein d'un échantillon de centaines de milliers de cellules, celles portant des mutations oncogènes.
On pourra ainsi utiliser cette information pour engager un traitement contre le cancer en réduisant considérablement les récurrences.
La généralisation de la biopsie liquide, qui permet de récupérer des cellules tumorales circulantes et ainsi recueillir un maximum d'informations sur la composition de la tumeur et sur son stade de développement, sans aucune intervention chirurgicale.
Grâce à la microfluidique, il sera possible de réaliser, dans des microgouttes, des millions de tests par heure. Ce procédé pourra être utilisé pour sélectionner des groupes de cellules produisant, par exemple, des anticorps très efficaces contre une bactérie.
L'exemple de la recherche de la meilleure arme antivirus
Première étape : on inocule le virus à un animal. Les cellules du système immunitaire de ce dernier - les lymphocytes B - réagissent en produisant des anticorps. Ceux-ci se combinent alors à des molécules spécifiques du virus, présentes à sa surface, appelées antigènes.
Deuxième étape : certains lymphocytes B, ayant une plus grande affinité avec les antigènes, produisent de meilleurs anticorps. Et c'est justement cette "élite" que l'on cherche à identifier.
On prélève alors du sang de l'animal pour récupérer les lymphocytes B, qui sont ensuite placés dans une solution nutritive et envoyés dans un canal de la plaque de microfluidique.
Ce canal va en croiser un autre dans lequel circule une huile avec un débit contrôlé. Les deux fluides ne pouvant se mélanger, l'huile va alors former un petit container, encapsulant une cellule unique, avec un peu de son liquide nutritif.
Troisième étape : chaque gouttelette devient alors un milieu d'essai avec son lymphocyte B, qui produira ses propres anticorps après quelques jours d'incubation. Ne reste plus aux chercheurs qu'à introduire les antigènes du virus cible et à détecter, au moyen d'un système optique, le lymphocyte B qui produit les anticorps les plus efficaces.
Ils peuvent alors séquencer le gène à l'origine de cet anticorps idéal et produire ainsi en masse la molécule thérapeutique la plus efficace.
La microfluidique pourrait révolutionner l'industrie pharmaceutique et la recherche de nouveaux médicaments en parvenant à tester des molécules 10 000 fois plus vite et pour 10 000 fois moins cher.
Elle pourra aussi créer de nouveaux systèmes de délivrance beaucoup plus performants.
Les organes sur puce progressent grâce aux avancées sur les cellules souches.
Le prochain objectif est de créer un système dans lequel tous les organes humains sont connectés par des capillaires sanguins microfluidiques, représenté dans le schéma ci-dessous.
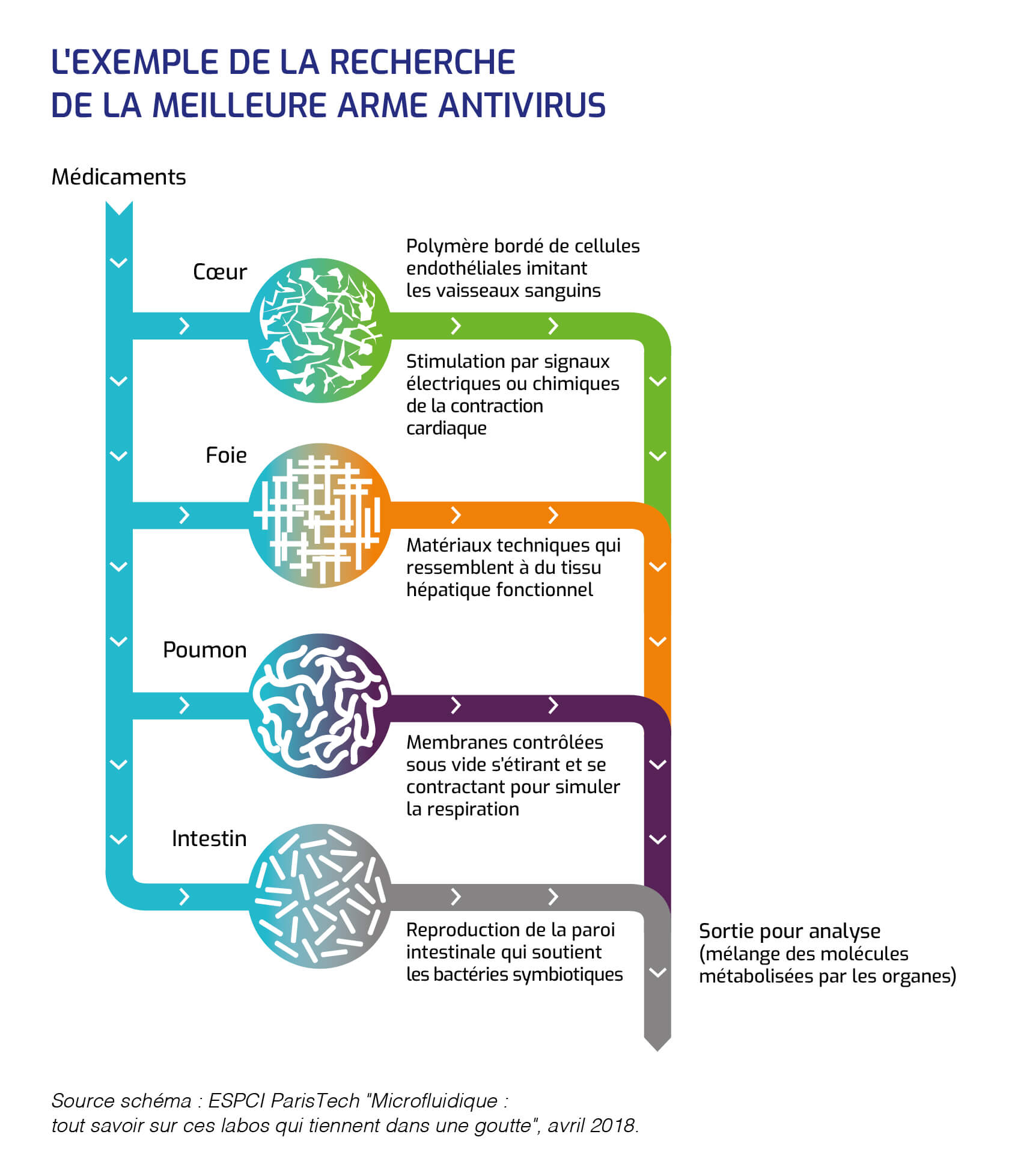
Enfin, l'importance du confinement ayant été soulignée dans le développement de réactions biochimiques conduisant à la naissance de la vie, la microfluidique, couplée à la biochimie, est aujourd'hui la technologie la plus adaptée pour proposer un scénario sur l'origine de la vie.
Ce qui est en cours
La microfluidique représente pour la biologie et la chimie une révolution semblable à celle apportée par les microprocesseurs à l'électronique et l'informatique.
Quelques chiffres clés
• Aujourd'hui, un très grand nombre de sociétés développent la technologie microfluidique. Plus de 250 entreprises et 10 000 chercheurs travaillent dans ce champ de par le monde.
• Le marché de la microfluidique est évalué à 6 milliards de dollars par an.
• A titre d'exemple, le marché de la cellule unique, fortement impacté par la microfluidique, est évalué à 1 milliard de dollars.
Place de la France : la France fait partie des nations leaders du domaine
400 personnes
50 laboratoires
50 start-up
Un institut phare : l'Institut Pierre-Gilles de Gennes
La microfluidique ou l'art de manipuler des volumes de fluides minuscules à l'aide des nouvelles technologies
Parlant du monde de l'industrie et celui de la recherche scientifique, Pierre-Gilles de Gennes se plaisait à dire que "les deux ont tout à gagner à travailler ensemble".
Des frontières entre les disciplines scientifiques, il répétait qu'il fallait savoir s'en affranchir pour les rendre plus fécondes et en tirer tout le potentiel.
C'est dans cet esprit que l'Institut Pierre-Gilles de Gennes (IPGG) a été créé : réunir autour d'une thématique transdisciplinaire (la microfluidique) des expertises complémentaires (physiciens, biologistes, chimistes, technologues) pour développer la recherche fondamentale et faire éclore des applications dans la santé, l'énergie, l'agro-alimentaire, la cosmétique, l'instrumentation... Vingt start-up y sont incubées. www.institut-pgg.fr
La microfluidique est déjà une réalité : elle permet aujourd'hui d'effectuer des analyses complexes dans une simple goutte et d'injecter des produits plus facilement dans le corps humain.
Quelques exemples :
• Le laboratoire sur puce peut, à partir d'une goutte de sang, diagnostiquer la réalité d'une crise cardiaque. Le diagnostic est délivré en quinze minutes, alors que les systèmes traditionnels nécessitaient plus d'une dizaine d'heures.
• La puce pour le génotypage permet l'identification d'un objet (par exemple un virus) à partir de séquences caractéristiques de gènes, mais aussi l'identification d'ARN et de protéines.
• Les puces de diagnostic de pathogènes utilisent un échantillon corporel, permettant de déterminer la présence d'un virus, bactérie ou micro-organisme en quelques minutes, et à très bas coût.
• Le test sanguin équipé d'une puce électronique permet désormais de détecter simultanément en vingt minutes le virus du sida, la syphilis et une dizaine d'autres maladies infectieuses (hépatites B et C, herpès.).
• Les micropompes permettent d'injecter un produit dans le corps humain. La pompe d'injection d'insuline dans le foie, pour le traitement du diabète, est plus efficace et confortable pour le malade.
La microfluidique permet des percées dans le domaine du cancer par la modélisation de certains organes (foie, rein, poumon, intestin).
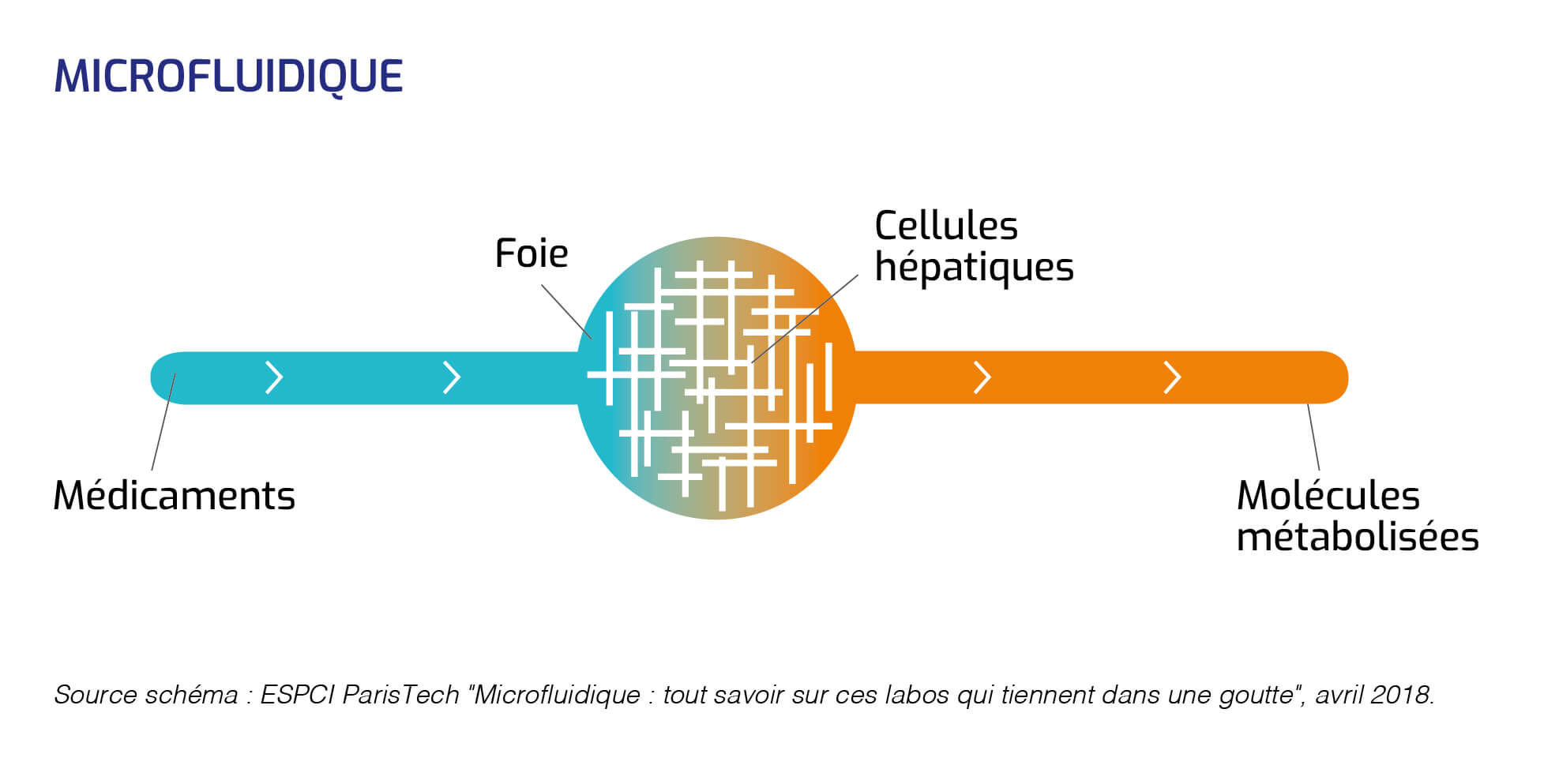
L'enjeu pour la microfluidique est de parvenir à reproduire la vascularisation de ces organes et de tous les transferts entre le fluide de vascularisation et les tissus internes de l'organe ; des prototypes sont actuellement utilisés dans cette perspective.

Ce qu'il faut dépasser
-
Des verrous scientifiques
Ils tiennent :
1. aux limites des capacités de manipulation des fluides, qui, bien que puissantes, doivent encore progresser ;
2. aux limites de réalisation de systèmes microfluidiques complexes, permettant de mimer la complexité du vivant, dans le domaine des organes sur puce ou la gestion des fluides dans les mémoires ADN.
Ils nécessitent :
1. une prise de conscience et des soutiens permettant à la France de faire progresser son leadership ;
2. de réconcilier recherche et entreprise, de manière à produire un effet stimulant pour les chercheurs en quête d'aventure ;
3. de développer le tissu de start-up et prendre les risques permettant l'émergence de leaders mondiaux.
Fiche réalisée avec l'appui de Patrick Tabeling, directeur de l'Institut Carnot IPGG (Institut Pierre-Gilles de Gennes) Microfluidique.
Extrait de Santé 2030 - Partie 2 : les vecteurs d'innovation.
Retrouvez l'intégralité de l'étude sur le site.

